생명연, 인간 줄기세포로 만든 ‘장(腸) 모델’로 약물 위장관 독성 94% 정확도로 예측
인간의 장(腸) 구조와 기능을 정밀하게 재현한 줄기세포 기반 세포 모델로 약물이 유발하는 위장관 독성을 세포가 죽기 전 단계에서 실시간으로 감지하는 평가 플랫폼이 개발됐다.
한국생명공학연구원(원장 권석윤) 국가아젠다연구소 손미영 박사 연구팀은 인간 다능성 줄기세포(체내 모든 세포로 분화할 수 있는 세포)로부터 만든 정상 장 상피세포 모델(hIEC)을 구축하고, 항암제·표적치료제·소염진통제 등 임상 약물 17종을 대상으로 검증한 결과 위장관 독성 예측 정확도 94%를 달성했다고 5일 밝혔다. 이번 성과는 기초의학 분야 국제 학술지 ‘Experimental & Molecular Medicine'(영향력지수 12.8) 온라인판에 2월 12일 게재됐다.
왜 기존 방식으론 약물의 장 독성을 제대로 잡지 못했나
신약을 개발할 때 가장 빈번하게 나타나는 부작용 중 하나가 위장관 독성이다. 항암제를 비롯한 다양한 약물이 구토, 설사, 점막염(장 내벽이 헐고 염증이 생기는 증상) 등을 유발하며, 이는 임상시험 도중 치료 중단이나 용량 감소로 이어져 신약 개발 실패의 주요 원인이 된다. 특히 장의 보호 기능이 먼저 약해진 뒤 염증과 조직 손상으로 진행되는 경우가 많아, 초기 변화를 빠르게 포착하는 것이 매우 중요하다.
그러나 지금까지 전임상(동물실험 및 세포실험 단계) 독성 평가에는 주로 ‘Caco-2’라는 세포가 쓰여 왔다. Caco-2는 인간 대장암에서 유래한 세포주(실험실에서 반영구적으로 증식시킨 세포 집단)로, 장 흡수 연구에 수십 년간 활용돼 왔다. 하지만 암세포에서 유래했기 때문에 정상적인 사람 장의 세포 구성과 기능을 충분히 반영하지 못한다는 구조적 한계가 있었다.
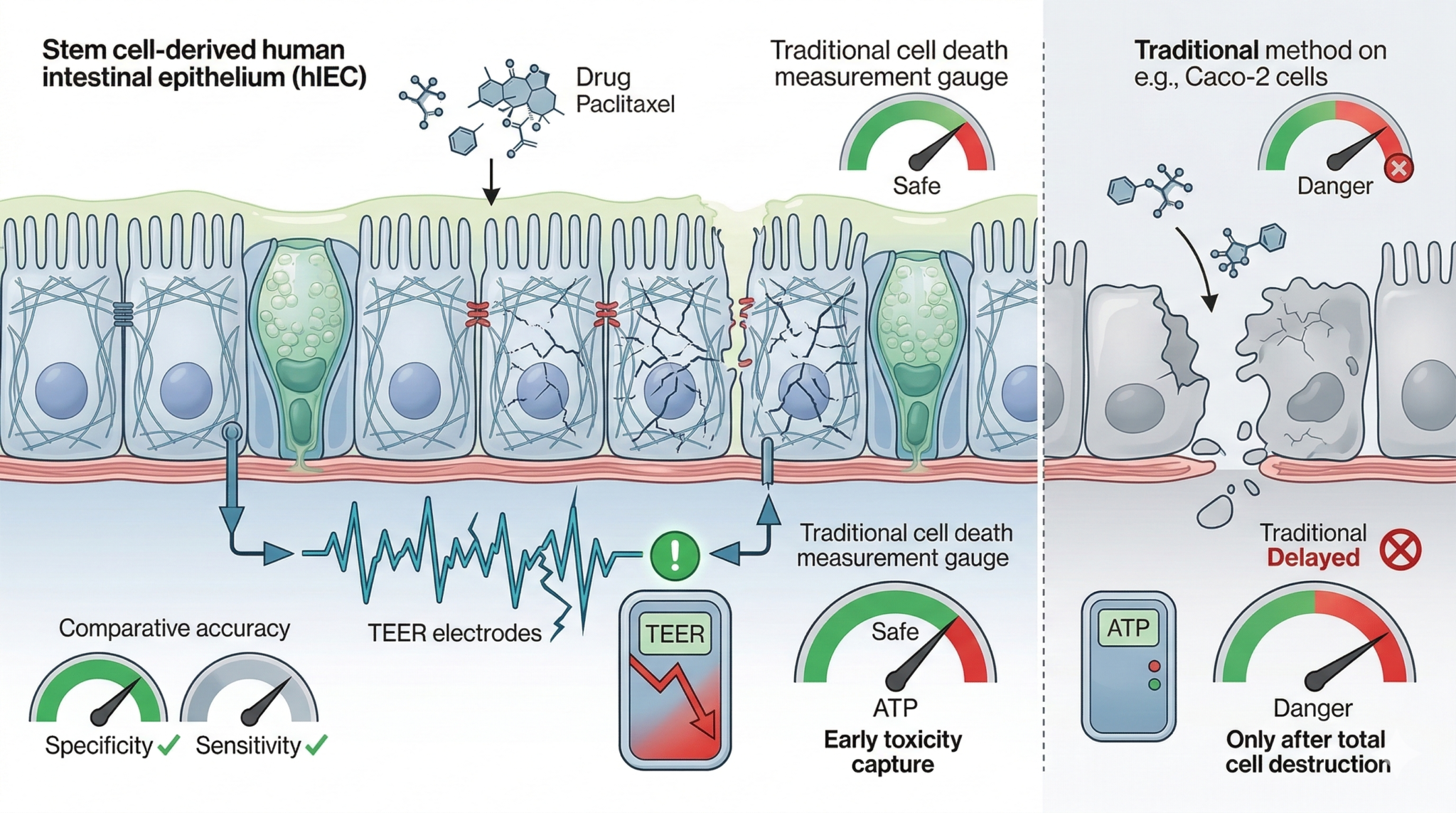
더 큰 문제는 기존 평가법의 측정 방식 자체에 있었다. 대부분의 독성 평가는 ATP(세포 에너지원) 측정을 통해 세포 생존 여부를 확인하는 방식에 의존했다. 이 방법은 세포가 완전히 죽어야 이상 신호를 포착할 수 있어, 세포는 살아 있지만 장벽 기능이 이미 무너지고 있는 ‘초기 독성 신호’를 놓칠 수밖에 없었다.

사람 장과 똑같이 만들어, 세포 죽기 전에 잡는다
연구팀이 개발한 hIEC(human Intestinal Epithelial Cells, 인간 장 상피세포) 모델은 인간 다능성 줄기세포로부터 분화시킨 정상 장 세포로 구성된다. 영양분을 흡수하는 흡수세포, 장을 보호하는 점액을 분비하는 배상세포(Goblet cell) 등 실제 소장 상피를 이루는 여러 종류의 세포가 함께 포함되어 있어 사람의 장 환경을 실험실에서 정밀하게 재현할 수 있다.
이 모델의 핵심 평가 도구는 TEER(Transepithelial Electrical Resistance, 경상피 전기저항)다. 장 상피 세포층은 세포와 세포 사이를 ‘밀접접합(tight junction)’이라는 단단한 결합으로 묶어 외부 물질이 함부로 혈액 속으로 들어오지 못하게 막는 장벽 역할을 한다. TEER는 이 장벽의 온전함을 전기 저항값으로 측정하는 지표로, 장벽이 손상될수록 저항값이 낮아진다. 세포가 죽기 전에도 이 값이 먼저 떨어지기 때문에 독성의 초기 신호를 민감하게 포착할 수 있다. hIEC 모델의 TEER 값은 기존 Caco-2보다 실제 사람 장과 훨씬 유사한 수준을 나타냈다.
17종의 임상 약물을 적용한 검증 실험에서 이 플랫폼은 94%의 전체 예측 정확도를 달성했다. 특히 특이도(Specificity, 실제로 독성이 없는 약물을 정확하게 ‘안전’으로 판정하는 비율) 100%를 기록해, 안전한 약물을 위험하다고 잘못 판정하는 오류를 완전히 없앴다. 또한 기존 방식으로는 독성을 확인하기 어려웠던 항암제 파클리탁셀(Paclitaxel) 등에서 초기 장벽 손상을 92%의 민감도로 포착하는 데 성공했다.
세포 뼈대가 무너지면 장벽이 먼저 쓰러진다
연구팀은 약물이 장벽을 손상시키는 분자 수준의 원리도 함께 규명했다. 대표적인 미세소관(세포 내부를 지지하는 골격 구조) 안정화 항암제인 파클리탁셀과 도세탁셀(Docetaxel)을 처리한 뒤 전사체 분석(RNA-seq, 세포 안에서 어떤 유전자가 얼마나 활성화되어 있는지를 총망라해 분석하는 기술)을 수행한 결과, 두 약물 모두에서 공통적인 패턴이 확인됐다.
세포의 형태를 유지하고 세포 사이를 단단히 연결하는 역할을 하는 세포골격(Cytoskeleton) 및 세포접착(Cell adhesion) 관련 유전자들의 활성이 급격히 낮아진 것이다. 즉, 세포 자체는 아직 살아 있어도 세포를 지탱하는 뼈대가 먼저 무너지면서 장벽 기능이 붕괴된다는 사실을 분자 수준에서 과학적으로 증명한 것이다. 이는 장 독성이 단순한 세포 사멸의 문제가 아니라 구조적 붕괴에서 시작된다는 새로운 기전을 제시한다.
연구책임자 손미영 박사는 “이번 연구는 실제 인간의 장 기능을 정밀하게 모사한 모델을 통해 약물 유발 장 손상을 높은 정확도로 예측할 수 있음을 보여준 사례”라며, “향후 환자 맞춤형 오가노이드(실험실에서 줄기세포를 3차원으로 배양해 만드는 소형 인공 장기) 기반 장 독성 정밀 예측 플랫폼으로 확장해 나갈 계획”이라고 밝혔다.