STEPHANIE ARNETT/MITTR | CDC, ENVATO
Three people were gene-edited in an effort to cure their HIV. The result is unknown.
유전자 편집 기술로 에이즈를 치료할 수 있을까?
크리스퍼 유전자 가위로 에이즈의 원인 바이러스인 HIV를 제거하려는 임상험이 세 명의 환자를 대상으로 수행됐다.
유전자 편집 기술인 크리스퍼(CRISPR) 유전자 가위는 인간 아기의 유전자를 바꾸고, 동물을 변형시키고, 낫적혈구병(겸상적혈구병)을 가진 사람을 치료하는 데 사용되어 왔다.
이제 과학자들은 새로운 시도에 도전하고 있다. 바로 크리스퍼를 이용해서 에이즈의 원인 바이러스인 HIV를 영구적으로 치료하는 것이다.
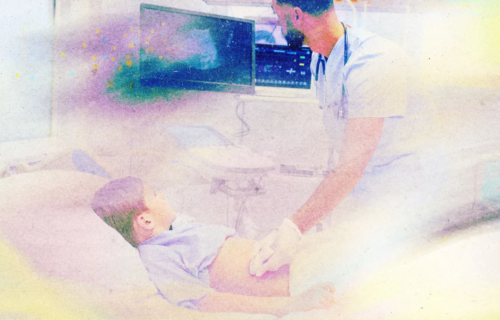
샌프란시스코에 본사를 둔 생명공학 기업 익시전 바이오테라퓨틱스(Excision BioTherapeutics, 이하 ‘익시전’)는 이 놀라운 실험을 통해 HIV 감염자 세 명의 신체에 크리스퍼를 사용해서 바이러스가 숨어 있는 곳을 잘라내고 파괴하도록 명령했다고 밝혔다.
익시전의 궁극적인 목표는 유전자 편집 약물을 정맥에 주사해서 단 한 번의 주사로 HIV 감염을 치료하는 것이며, 이번 초기 단계 연구는 그러한 목표 달성을 위한 조사 단계에 해당한다. 익시전에 따르면 첫 번째 환자는 약 1년 전에 이 치료를 받았다.
해당 연구에 참여한 의사들은 10월 25일 브뤼셀에서 열린 회의에서 이 치료법이 안전하고 큰 부작용이 없는 것으로 보인다고 보고했다. 그러나 치료 효과에 대한 초기 데이터는 공개하지 않았기 때문에 외부 전문가들은 치료 효과에 대해서 추측할 수밖에 없다.