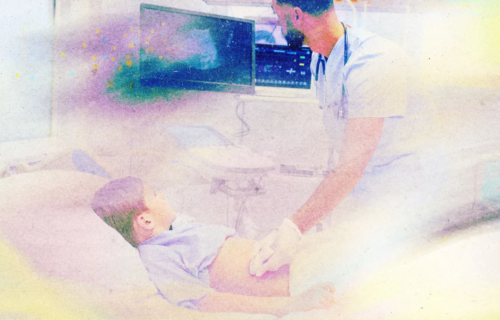
정희원 서울아산병원 노년내과 전문의
10년 안에 노화를 거꾸로 되돌리는 시대 도래한다
기대 수명이 90세가 넘는 시대에 살고 있다. 장수가 더 길고 건강한 삶을 보장할 수 없다면, 어떤 노후를 보내느냐는 전적으로 자신의 의지에 달렸다. 서울아산병원 노년내과 정희원 교수를 만나 노화와 노인의학에 대한 궁금증을 풀어보았다.
정희원 교수는 의과대학 시절, 응급실에 실려 온 환자가 처방 약 중 일부를 빼자 며칠 만에 멀쩡해지는 모습을 보고 노인의학에 매료되었다. 그는 “성인 중심의 전문 진료과가 약을 추가해서 환자를 치료하는 게 일반적이라면, 노인의학은 환자의 약을 빼면서 환자를 치료할 수 있다는 것이 굉장히 신선하게 느껴졌다”고 말한다. 나이가 들면 장기나 기관의 기능이 저하되는 노쇠가 온다. 정희원 교수는 “노쇠는 사람의 회복 탄력성이 떨어져 있다는 의미인데 이런 사람들이 약을 계속 추가할 경우, 예측할 수 없는 문제가 생길 수 있다”고 덧붙였다. 노년내과 같은 노인의학과(geriatics)에서는 노인의 특징적인 문제에 깊이 관여하여 환자의 전체적인 상태와 먹는 약, 신체와 인지 등 전반적인 기능을 고려해서 ‘환자 중심’ 치료 계획을 세운다. 보통 질병에 따른 진단과 치료 중심 의학과 구별되는 점이다.