질병관리청·국립보건연구원, 치명률 최대 75% 니파바이러스 국산 백신 개발 착수
치명률이 최대 75%에 달하며 현재까지 상용화된 백신이 없는 고위험 감염병 니파바이러스를 겨냥한 국산 백신 개발이 본격 추진된다.
질병관리청(청장 임승관) 국립보건연구원(원장 남재환)은 고위험 인수공통감염병인 니파바이러스 감염증에 선제적으로 대응하기 위해 국내 기업과 협력해 재조합 단백질 및 mRNA 플랫폼을 병행 적용한 니파바이러스 백신 개발을 본격 추진한다고 지난 6일 밝혔다. 올해 동물모델 효력평가와 GMP 생산공정 확립을 시작으로, 안전성 평가(2027~2028년)와 임상 1상 시험(2029~2030년)을 거쳐 국산 백신을 확보하는 것이 목표다.
치명률 최대 75%…백신도 치료제도 없는 ‘팬데믹 후보’ 바이러스
니파바이러스(Nipah virus)는 과일박쥐를 자연 숙주로 하는 RNA 바이러스로, 감염된 동물이나 사람과의 접촉을 통해 전파되며 사람 간 전파도 가능한 고위험 인수공통감염병이다. 인수공통감염병이란 동물과 사람 사이에서 서로 전파될 수 있는 감염병을 의미한다. 니파바이러스에 감염되면 뇌염과 호흡기 질환 등 심각한 증상이 나타나며, 치명률이 40~75%에 이르는 것으로 보고되고 있다. 이는 코로나19의 초기 치명률을 크게 웃도는 수준으로, 만약 대규모 유행이 발생할 경우 그 피해가 막대할 수 있다.
현재까지 니파바이러스에 대해 상용화된 백신이나 치료제는 존재하지 않는다. 세계보건기구(WHO)와 감염병혁신연합(CEPI)은 니파바이러스를 미래 팬데믹을 일으킬 가능성이 있는 감염병으로 분류하고 우선적인 대응을 촉구하고 있다. CEPI는 Coalition for Epidemic Preparedness Innovations의 약자로, 신종 감염병 백신 개발을 지원하기 위해 설립된 국제기구다.
현재 해외에서는 여러 기관이 다양한 플랫폼으로 임상시험을 진행 중이다. 아우로백신(AuroVaccines)이 개발한 재조합 단백질 백신 HeV-sG-V는 임상 1상을 완료했으며, 공중보건 백신(Public health vaccines)의 바이럴벡터 백신 PHV02도 임상 1상을 완료하고 추가 실험을 진행 중이다. 바이럴벡터 백신이란 무해하게 처리한 바이러스를 운반체로 활용해 항원 유전 정보를 세포 안으로 전달하는 방식이다. NIAID(미국 국립알레르기전염병연구소)와 모더나가 공동 개발 중인 mRNA 기반 백신(mRNA-1215)은 임상 1상이 진행 중이며, NIAID와 옥스퍼드 대학교가 개발한 바이럴벡터 백신 ChAdOx1 NiVvaccine은 임상 1상을 마치고 2상에 진입한 상태다.
임승관 질병관리청장은 “니파바이러스는 현재 지역적으로 발생하고 있으나 미래 팬데믹으로 확산될 잠HeV-sG-V(아우로백신)재적 위험이 존재한다”며 “앞으로도 국내 기업 등과 협력을 확대하여 신변종 감염병에 대한 선제적 대응체계를 지속적으로 고도화해 나갈 계획”이라고 밝혔다.
재조합 단백질·mRNA 두 가지 플랫폼 병행 개발
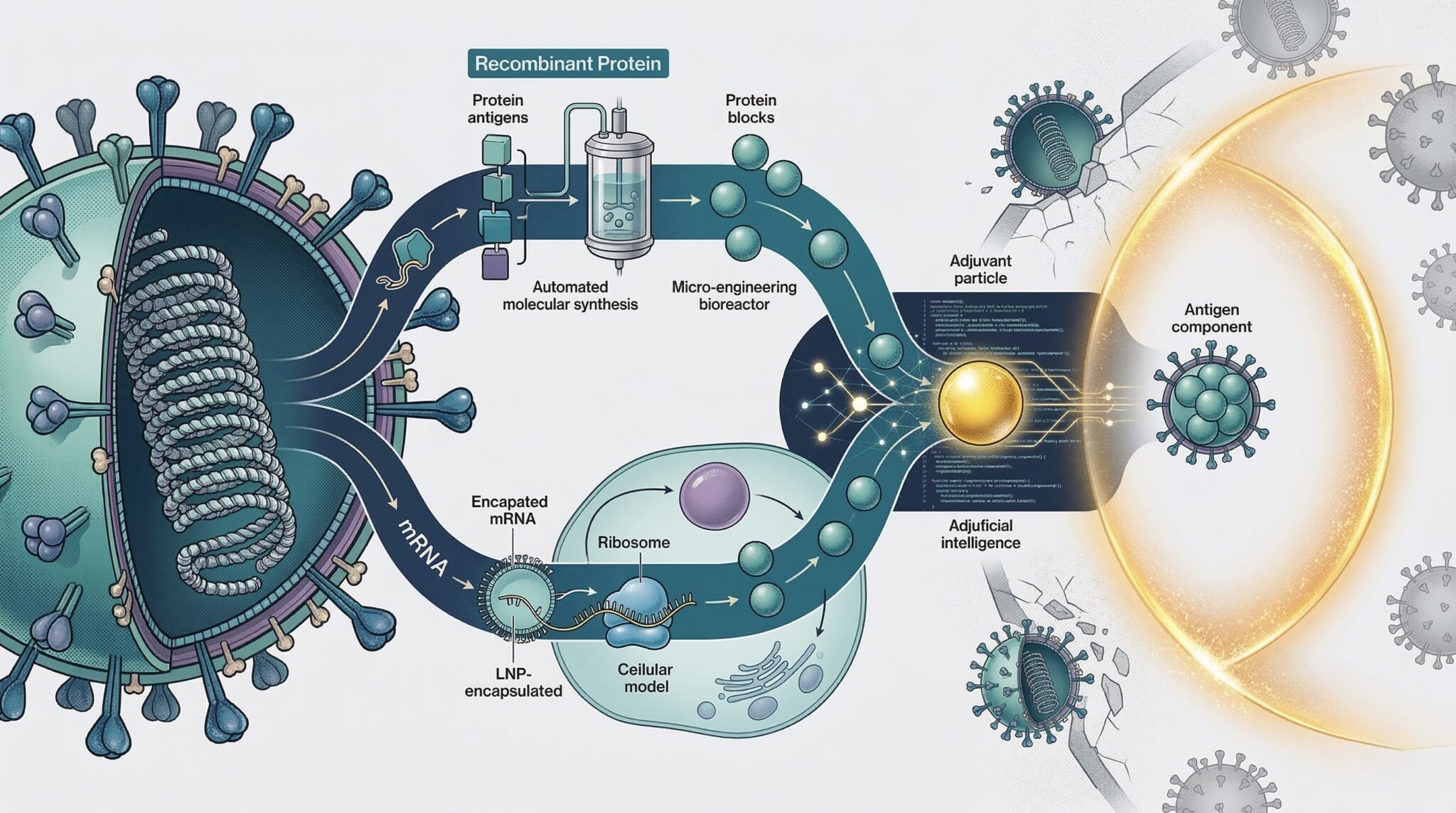
이번 국산 니파바이러스 백신 개발은 두 가지 플랫폼을 병행하는 전략을 택했다. 하나는 재조합 단백질 방식으로, 바이러스의 특정 단백질 조각을 인공적으로 만들어 면역 반응을 유도하는 전통적인 백신 제조 방식이다. 다른 하나는 mRNA 플랫폼으로, 세포가 바이러스 단백질을 스스로 만들도록 유전 정보를 전달해 면역을 유도하는 차세대 기술이다. mRNA 백신은 코로나19 팬데믹을 계기로 빠른 개발 속도와 유연성이 입증된 플랫폼이다. 두 방식을 동시에 추진함으로써 하나의 경로에서 문제가 생기더라도 다른 경로로 개발을 이어갈 수 있는 리스크 분산 전략이기도 하다.
여기에 면역증강제 플랫폼과 인공지능 기술도 적용된다. 면역증강제(adjuvant)란 백신의 면역 반응을 강화하기 위해 함께 투여하는 보조 성분으로, 같은 양의 항원으로도 더 강하고 지속적인 면역 반응을 이끌어낼 수 있다. 질병관리청은 확보한 백신 후보물질과 국내 기업의 기술 역량을 결합해 이들 기술을 체계적으로 적용할 방침이다.
이번 개발은 2022~2023년에 완료한 기반연구 단계에서 백신 후보물질 발굴을 마치고, 현재는 비임상시험 단계를 진행 중인 상태다. 2024~2026년에는 백신 후보물질 효능평가를 수행하고 있으며, 올해는 그보다 한 단계 나아가 동물모델 효력평가와 재조합 단백질 기반 GMP(우수의약품 제조 및 품질관리 기준) 생산공정 확립에 본격 착수한다. GMP란 의약품의 안전성과 유효성을 보장하기 위해 제조 전 과정에 적용되는 국제 품질관리 기준으로, 임상시험용 의약품 생산에 필수적인 요건이다.

2030년 임상 1상 진입 목표…단계별 검증 로드맵 제시
질병관리청이 제시한 개발 로드맵은 크게 다섯 단계로 구성된다. 기반연구(2022~2023년)와 기초 비임상시험(2024~2026년)을 거쳐, 올해부터는 TRL4 단계 비임상시험으로 동물모델 효력평가와 재조합 단백질 기반 GMP 생산을 추진한다. mRNA 기반 니파바이러스 안전성 평가는 2026~2027년에 걸쳐 진행될 예정이다. TRL(Technology Readiness Level)은 기술 성숙도를 나타내는 지표로, TRL4는 실험실 수준의 생체 내 안전성과 유효성을 확보하는 단계를 의미한다.
이후 2027~2028년에는 TRL5 단계로 재조합 단백질 독성평가를 수행한다. TRL5는 GLP(우수실험실 기준) 비임상연구와 임상용 GMP 공정 확립 단계에 해당한다. GLP란 비임상 안전성 시험의 신뢰성을 보장하기 위한 국제 기준으로, 이 단계를 통과해야 임상시험 신청이 가능하다. 이 모든 단계를 거쳐 2029~2030년에 임상 1상 시험에 진입하는 것이 최종 목표다.
백신연구개발총괄과 이유경 과장은 “국내 기술 기반의 백신 후보물질과 제조 플랫폼을 선제적으로 확보함으로써 국산 백신 개발 역량을 한층 강화해 나가겠다”고 밝혔다. 한편 이번 니파바이러스 백신 개발은 질병관리청이 2023년 수립한 「신종감염병 대유행 대비 중장기계획」에서 선정한 백신 개발 우선순위 감염병 9종 중 하나로, 코로나19·인플루엔자·SFTS·치쿤구니아·RSV·신증후군유행성출혈열(한탄)·라싸·뎅기와 함께 국내 기술 기반의 백신 개발이 다각적으로 추진되고 있다.