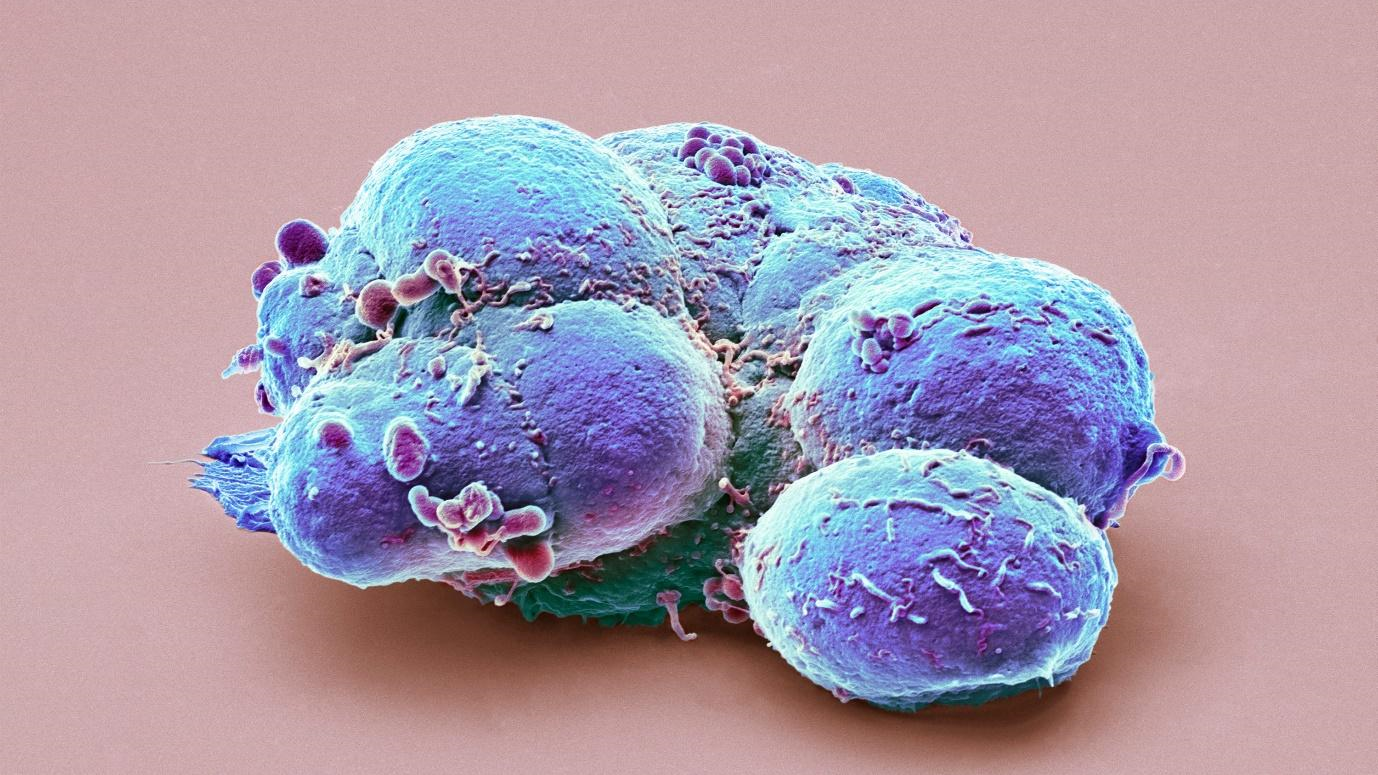
STEVE GSCHMEISSNER/SCIENCE PHOTO LIBRARY
After 25 years of hype, embryonic stem cells are still waiting for their moment
줄기세포 연구 25년, 역사는 지금도 쓰여지고 있다
25년 전 커다란 논쟁을 불러일으키며 등장한 배아줄기세포 기술은 여러 의학적 난관에 부딪히고 정치 논쟁에 휘말리며 개발이 지연됐다. 하지만 이제 과학자들은 줄기세포 치료법 개발에 조금씩 가까워지고 있다.
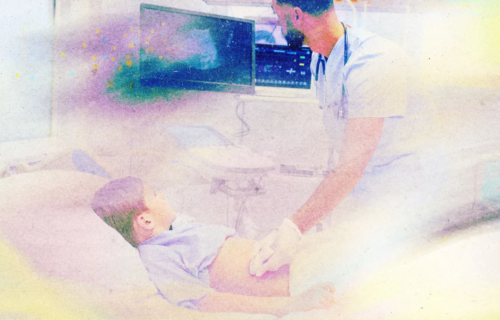
지금으로부터 25년 전인 1998년 미국 위스콘신의 한 연구진이 인간 배아로부터 다능성 줄기세포를 분리하는 데 성공했다. 인체 발달의 시작점인 줄기세포는 심근세포, 신경세포 등 우리 몸을 구성하는 다양한 세포로 자랄 수 있는 잠재력을 가지고 있어 생물학의 주요 돌파구로 여겨졌다.
훗날 <내셔널 지오그래픽>은 이 놀라운 가능성에 대해 ‘병든 장기와 조직을 살아 있는 새것으로 대체하는 의료 혁명을 일으킬 꿈’이라고 요약했다. 줄기세포는 새로운 시대의 서막이자 궁극적인 목표였으며, 매체에서는 이에 온갖 화려한 수식어를 갖다 붙였다.
하지만 20여 년이 지난 오늘날 줄기세포를 기반으로 한 치료법은 시중에 나와 있지 않다. 단 한 개도 없는 것이 현실이다.
필자는 이렇게 된 이유를 살피기 위해 2023년 6월 국제줄기세포학회(International Society for Stem Cell Research, 이하 ISSCR) 연례학술대회에 참석했다. 수백 명의 생물학자들이 모인 학회장의 한쪽 벽에는 현미경으로 본 세포의 흑백 사진이 거대한 스크린에 다소 위협적으로 띄워져 있었다. 그 속에는 팔을 뻗은 것처럼 털이 있는 둥근 모양의 세포들이 있는가 하면, 모래알 같은 기이한 물질로 채워진 직사각형 단면 모양의 세포들도 있었다. 주제곡으로 록 밴드 휴이 루이스 앤 더 뉴스(Huey Lewis and the News)의 ‘난 새 약을 원해(I Want a New Drug)’가 흘러나왔다.