GETTY IMAGES
This company plans to transplant gene-edited pig hearts into babies next year
유전자 조작 돼지의 심장을 소아 환자에 이식하려는 스타트업
미국의 생명공학 기업 이제네시스(eGenesis)가 유전자를 편집한 돼지의 심장을 새끼 개코원숭이에 이식하기 시작했다. 이르면 내년, 사람을 대상으로 같은 연구가 추진될 수 있다.
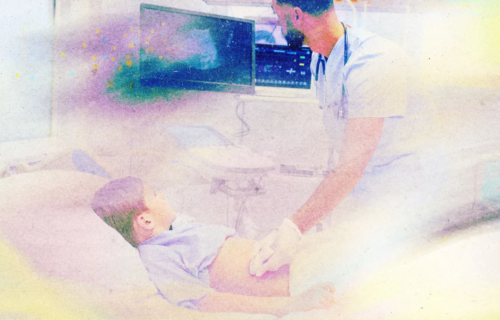
엘리 카츠(Eli Katz)가 줌(Zoom) 화면 너머로 사진 한 장을 보여주며 말했다. 사진 속 새끼 개코원숭이는 가운을 입고 똑바로 앉아있는 듯한 모습이었다. “이 작은 아가씨는 꽤 침착해 보인다.”
생명공학 기업 이제네시스(eGenisis)의 최고의료책임자(CMO)인 카츠는 이 원숭이가 유전자 편집 돼지로부터 심장을 이식받은 최초의 개코원숭이이며, 앞으로 인간 아기에게 돼지 심장을 이식하기 위한 연구의 일환으로 수술이 진행됐다고 말했다.
매사추세츠 케임브리지에 본사를 둔 이제네시스는 유전자 편집 기술인 크리스퍼(CRISPR)를 이용해 돼지 유전체를 70회가량 수정하는 기술을 개발했다. 연구진은 돼지의 유전체를 편집하여 인간에게 성공적으로 돼지의 장기를 이식할 수 있다고 본다. 이 회사는 이르면 내년부터 심장에 심각한 결함이 있는 소아 환자에게 돼지 심장을 이식하기를 희망하고 있다. 이들의 목표는 아기들이 사람의 심장을 이식받기 전까지 시간을 벌어주는 것이다.
그에 앞서 이제네시스는 12마리의 새끼 개코원숭이로 이식을 연습할 예정이다. 현재까지 두 차례의 수술이 진행되었지만, 수술받은 두 마리 모두 며칠을 넘기지 못하고 죽었다.