DGIST, 우울증 약 효과 지연 메커니즘 세계 최초 규명…신경펩타이드 회로 재건 과정 밝혀
항우울제가 효과를 내기까지 수주에서 수개월이 걸리는 수수께끼가 풀렸다.
DGIST(총장 이건우) 뇌과학과 오용석 교수팀이 항우울제 투여 시 실제 치료 효과가 나타나기까지 수주 이상의 시간이 걸리는 ‘치료 지연’ 현상의 핵심 원인을 세계 최초로 규명했다고 26일 밝혔다. 흔히 쓰이는 우울증 치료제(SSRI)는 복용 직후 뇌 속 세로토닌 농도를 높이지만, 환자가 실제 기분 개선을 느끼기까지는 수주에서 수개월이 걸린다. 학계에서는 이를 뇌 신경회로의 구조적 변화 때문으로 추정해왔으나, 구체적인 분자 기전은 그동안 베일에 싸여 있었다.
연구팀은 최신 유전체 분석 기술을 통해 뇌의 해마 속 ‘모시세포’가 항우울제 자극을 받으면 특정 유전자의 단백질 번역을 가속화해 신경펩타이드인 ‘PACAP’을 생산한다는 사실을 발견했다. 연구 결과는 분자정신의학 분야의 세계적 권위지인 《Molecular Psychiatry》에 게재됐다.
세로토닌은 ‘신호탄’, 진짜 주인공은 신경펩타이드
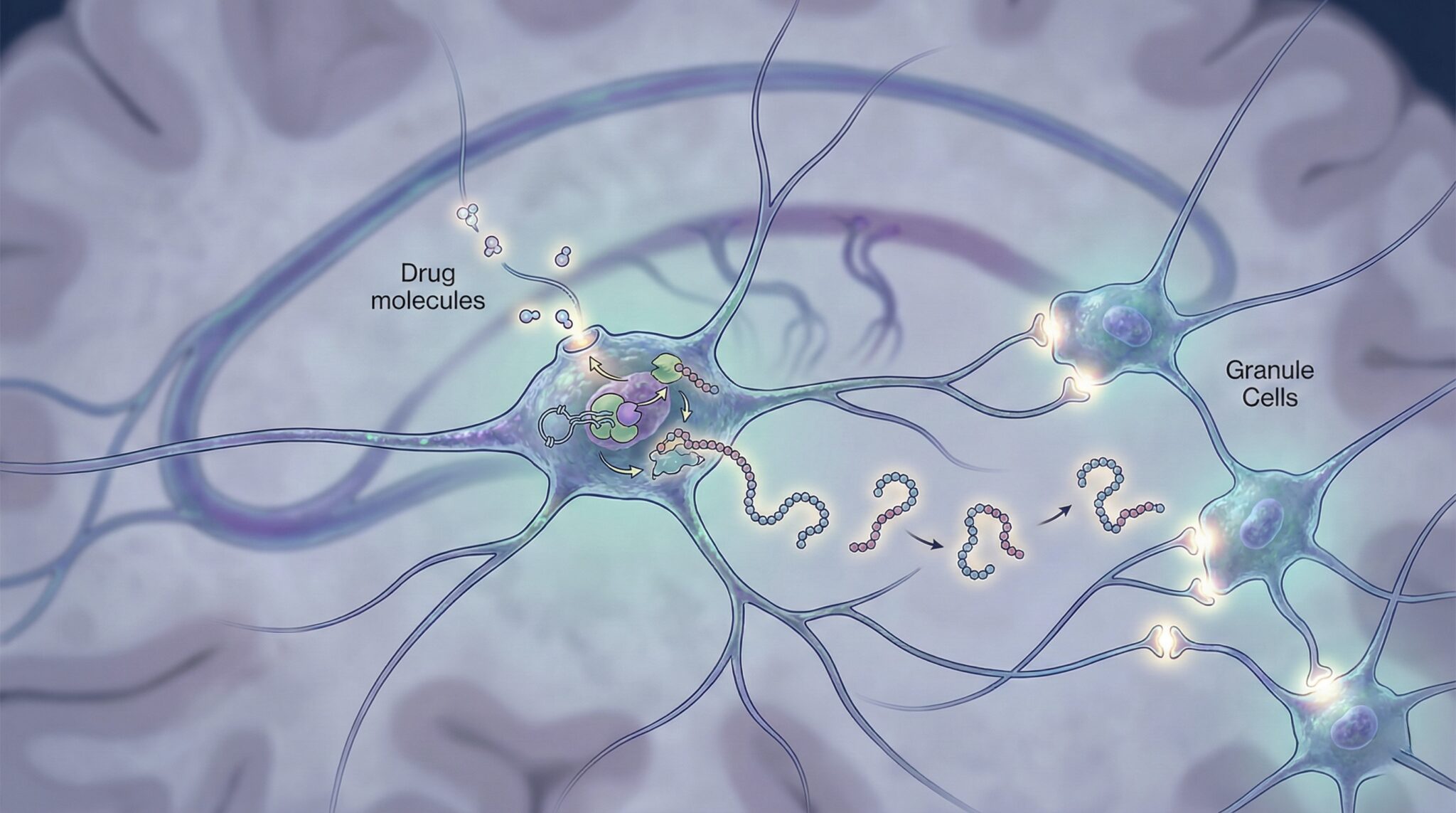
연구팀에 따르면, 약물을 복용해 세로토닌 수치가 올라가는 것은 일종의 ‘신호탄’에 불과하다. 실제 뇌를 치유하는 주인공은 ‘신경펩타이드’이며, 뇌가 이 펩타이드를 충분히 만들어내고 주변 신경세포를 재건하는 ‘회로 재프로그래밍’ 과정을 거쳐야만 비로소 항우울 효과가 나타나는 것이다. 신경펩타이드는 일반적인 신경전달물질보다 더 크고 복잡한 단백질성 신호 전달 물질로, 뇌 기능을 미세하게 조절한다. 이번 연구에서는 ‘PACAP’이라는 펩타이드가 우울증 회복의 결정적 열쇠임이 확인되었다.
오용석 교수팀은 최신 유전체 분석 기술을 통해 항우울제를 장기간 투여한 생쥐의 뇌 변화를 추적했다. 그 결과, 뇌의 해마 속에 있는 ‘모시세포(Mossy Cell)’가 항우울제 자극을 받으면 특정 유전자의 단백질 번역을 가속화해 신경펩타이드인 PACAP을 생산한다는 사실을 발견했다. 모시세포는 뇌의 해마 부위에서 기억과 감정을 조절하는 신경회로의 ‘관문’ 역할을 하는 세포로, 이번 연구에서 항우울제에 반응하는 핵심 사령탑임이 밝혀졌다.
연구팀은 Translating Ribosome Affinity Purification (TRAP)과 RNA 시퀀싱을 결합한 기법을 사용하여, 모시세포와 과립세포(Granule Cells) 간의 단백질 번역 양상 차이를 분석했다. 그 결과 만성적인 항우울제 투여는 모시세포에서만 선택적으로 번역 활성을 증가시키며, 이웃한 과립세포에서는 감지 가능한 변화가 없음을 확인했다. 이는 항우울제가 모든 신경세포에 동일하게 작용하는 것이 아니라, 특정 세포 유형에서만 선택적으로 반응을 유도한다는 것을 의미한다.
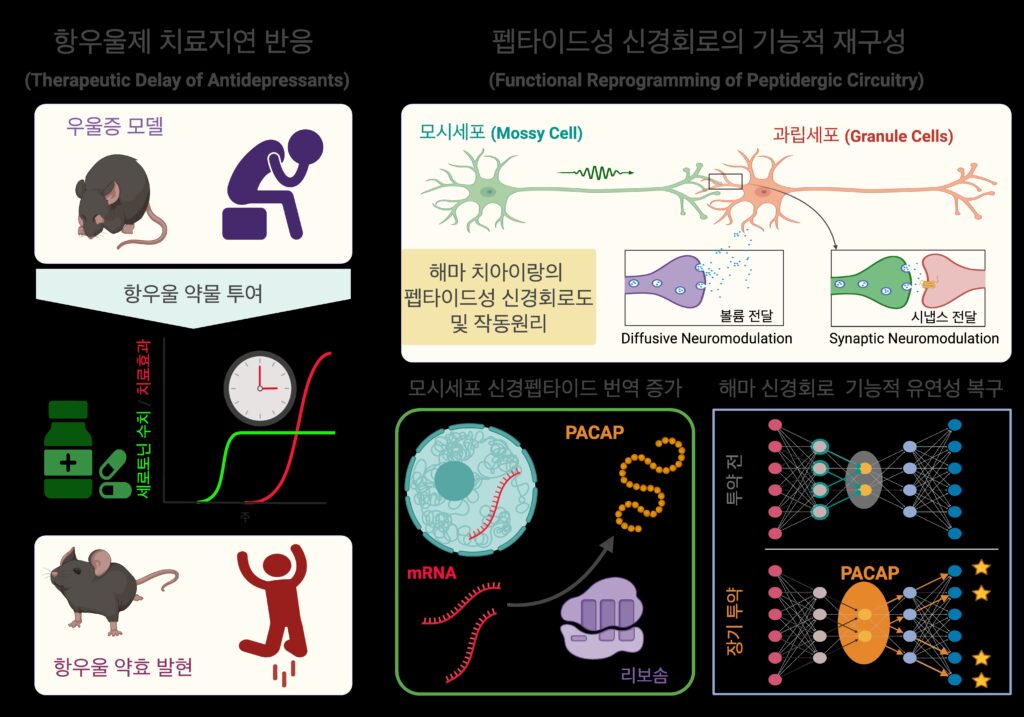
‘번역 재편성’ 과정 거쳐야 비로소 치료 효과
연구팀은 이 과정을 펩타이드 신경회로의 ‘번역 재편성(Translational Reprogramming)’이라고 명명했다. 번역 재편성은 세포 내 유전 정보를 단백질로 바꾸는 효율을 변화시켜 세포의 성질과 기능을 바꾸는 과정을 말한다. 즉, 항우울제를 복용하면 세로토닌이 즉시 증가하지만, 실제 뇌의 치유는 모시세포가 PACAP 펩타이드를 새롭게 만드는 번역 활성이 증가하고, 이 펩타이드가 해마의 표적세포로 전달되어 수용체에 의해 활성화되는 과정을 통해 뇌 신경회로가 건강하게 변화(가소성)해야만 일어난다.
연구팀의 실험 결과, PACAP 펩타이드는 PAC1 수용체를 발현하는 과립세포에 작용하여 신경적응 가소성을 매개하며, 이는 특히 장기간 항우울제를 투여받는 동안 행동 반응을 유도한다. 이러한 발견은 항우울제 작용을 전사 조절 중심 관점에서 확장하여, 신경세포 유형 특이적 번역 조절과 신경가소성의 상호작용이라는 새로운 기전으로 설명한 것이다. 기존에는 유전자 전사(DNA에서 RNA로 정보 복사) 수준의 조절에 주목했다면, 이번 연구는 번역(RNA에서 단백질로 합성) 수준의 조절이 항우울제 반응의 핵심임을 밝혀낸 것이다.
특히 흥미로운 점은 PACAP 펩타이드에 의한 항우울 메커니즘이 암컷 생쥐에서 훨씬 강력하게 작용한다는 것이다. 연구 결과에 따르면 PACAP의 기능은 수컷에 비해 암컷에서 더욱 두드러지게 나타났으며, 이는 PACAP이 항우울제 반응의 성별 차이를 설명할 수 있는 주요 분자적 인자임을 시사한다. 이는 남녀 간 우울증 발병 기전과 치료 반응의 차이를 설명하는 결정적 단서로, 향후 여성 환자에게 특화된 정밀 의료 치료법 개발에도 큰 기여를 할 것으로 보인다.
세로토닌 넘어 펩타이드 조절하는 속효성 치료제 개발 기대
이번 연구는 항우울제 개발의 새로운 방향을 제시한다. DGIST 뇌과학과 오용석 교수는 “우울증 치료가 늦어지는 이유를 신경펩타이드 생성 효율이라는 새로운 관점에서 풀어냈다”며, “앞으로는 세로토닌뿐만 아니라 신경펩타이드의 생성과 성숙 과정을 직접 조절해, 약을 먹자마자 즉각적인 효과를 내는 차세대 속효성 항우울제 개발 연구를 이어갈 계획”이라고 밝혔다.
이번 연구 성과는 여러 방면에서 활용될 수 있다. 항우울제 반응 예측 바이오마커 개발, 번역 조절 및 신경펩타이드를 표적으로 하는 차세대 항우울제 설계, 성차를 고려한 맞춤형 주요우울장애 치료 전략 수립 등에 직접적으로 활용할 수 있다. 특히 기존 항우울제가 효과를 내기까지 수주에서 수개월이 걸리는 한계를 극복할 수 있는 새로운 치료 전략의 기반을 마련했다는 점에서 의미가 크다.
다만 실용화까지는 몇 가지 과제가 남아 있다. 인간 뇌 또는 환자 유래 모델에서의 기전 검증, PACAP 번역 조절을 선택적으로 제어할 수 있는 약물 또는 분자 타깃 발굴, 장기 안정성 및 성별 차이에 대한 체계적인 검증이 필요하다. 연구진의 궁극적인 목표는 뇌 회로와 세포 수준에서 작동하는 번역 조절 메커니즘을 정밀하게 이해하고, 이를 실제 환자에게 도움이 되는 치료 전략으로 연결하는 것이다. 장기적으로는 성별과 개인 특성을 고려한 정밀 항우울 치료법을 확립해, 주요우울장애 환자들이 더 빠르고 정확한 치료를 받을 수 있도록 기여하고자 한다.
한편, 이번 연구 성과는 과학기술정보통신부와 한국연구재단의 중견연구자지원사업 및 창의도전연구기반지원 사업의 지원으로 수행됐다.