UNIST, 백혈구 접착력 변화로 암 재발·항암제 약효 진단하는 칩 개발
칩의 미세관에 혈액을 흘려보내 항암제 약효와 암 재발 여부를 읽어낼 수 있는 기술이 개발됐다. UNIST 바이오메디컬공학과 강주헌 교수팀은 혈액 속 백혈구의 접착력 변화를 분석하는 방식으로 암 재발, 항암제 치료 반응 등을 모니터링할 수 있는 칩 기반 기술을 개발했다고 3일 밝혔다.
혈액 속의 암세포를 직접 찾아내는 기존 액체 진단 기술과 달리, 암 조직의 염증물질이 환자 백혈구 표면의 접착력을 증가시키는 원리를 이용한 기술이다. 머리카락보다 가는 미세관이 얽혀 있는 칩 안으로 혈액을 흘려보낸 뒤, 관에 부착된 백혈구 숫자를 자동 프로그램으로 읽어내는 방식이다.
실험에서 유방암이 진행 중인 쥐의 백혈구는 건강한 쥐의 백혈구에 비해 칩 내벽에 달라붙는 백혈구 숫자가 최대 40배 더 많은 것으로 나타났다. 연구 결과는 국제학술지 《바이오센서 & 바이오일렉트로닉스(Biosensors and Bioelectronics)》에 3월 1일 게재됐다.
‘암세포 대신 백혈구를 본다’, 염증 반응이 만드는 접착력의 비밀
기존 암 모니터링 방식은 크게 두 가지다. MRI, CT 같은 영상 검사는 눈에 보이는 크기의 종양을 찾는 데 강하지만, 몇 밀리미터 미만의 미세 전이는 놓치기 쉽다. 액체 생검(liquid biopsy·혈액에서 암세포나 암세포가 흘린 DNA 조각을 찾아내는 진단 기술)은 민감도가 높지만 비용이 매우 높고, 암세포 자체가 혈액에 거의 흘러나오지 않는 초기 단계에서는 검출이 어렵다는 한계가 있다. 이번 연구는 암세포를 직접 찾는 대신, 암이 환자 몸에 남긴 ‘흔적’—면역 반응의 변화—를 읽는 방식이다.
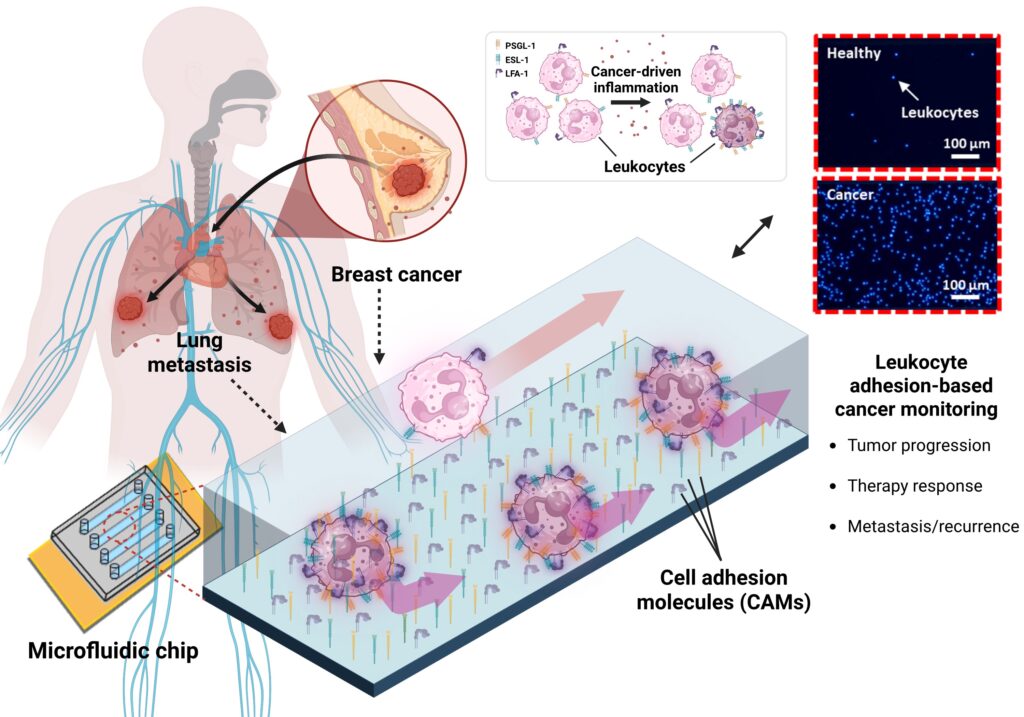
암 조직이 자라면서 주변에서는 지속적인 염증 반응이 일어난다. 이 과정에서 분비되는 염증성 물질은 혈액 속 백혈구(우리 몸의 면역세포로, 세균이나 바이러스가 침입하면 가장 먼저 달려가 제거하는 역할을 한다) 표면의 세포부착 수용체(cell adhesion molecule receptor·세포와 세포, 또는 세포와 혈관 내벽이 붙는 데 관여하는 분자)를 활성화시킨다. 이렇게 수용체가 활성화된 백혈구는 혈관 내벽을 따라 굴러가다 내벽에 더 단단히 달라붙어, 혈액의 흐름에도 내벽에서 떨어지지 않게 된다. 이를 ‘백혈구 유착(leukocyte adhesion·혈관벽을 따라 느리게 굴러다니는 롤링과 혈관벽에 달라붙는 부착으로 이뤄진 현상)’이라 부른다.
연구팀은 실제 혈관 내벽 환경을 재현한 생체모사 미세유체 칩을 제작했다. 칩의 미세관 안쪽에는 P-셀렉틴, E-셀렉틴, ICAM-1 등 염증 상황에서 혈관 내피에 나타나는 세포부착분자들을 코팅해, 백혈구가 실제 혈관에서 겪는 환경을 최대한 가깝게 구현했다. 이 칩에 혈액을 흘려보내 백혈구가 관 벽에 얼마나 달라붙는지를 직접 측정하고, 이를 정량 지표로 활용했다. 실험 결과, 4T1 유방암 세포를 주입한 쥐에서 암이 진행될수록(1~3주차) 칩에 부착하는 백혈구 수가 증가했으며, 특히 3주차에는 건강한 대조군 대비 최대 약 40배 증가가 관찰됐다.
항암제 약효는 즉각, 재발은 미세 단계부터: 백혈구 접착이 말해주는 것들
이 기술의 실용성은 항암치료 모델에서 확인됐다. 연구팀은 유방암이 이식된 마우스에 서로 다른 항암제를 투여한 결과, 실제로 종양 성장을 억제한 항암제(독소루비신)를 사용한 경우에는 칩 내벽에 부착되는 백혈구 수가 뚜렷하게 감소했다. 반면 항암 효과가 거의 없는 치료를 받은 경우에는 높은 백혈구 부착 수준이 그대로 유지됐다. 항암제의 실제 효능을 치료 시작 직후부터 즉각적으로 확인할 수 있다는 의미다.
더 주목할 점은 수술 후 재발 감지 능력이다. 원발 종양을 제거한 직후에는 암으로 인한 염증 신호가 줄어들면서 백혈구 부착 수가 일시적으로 감소했지만, 이후 전이나 재발이 발생한 마우스에서는 백혈구 부착 수가 다시 증가했다. 반대로 전이나 재발이 나타나지 않은 경우에는 낮은 수준이 유지됐다. 이는 육안이나 영상 진단으로는 확인되지 않는 미세 전이가 시작되는 단계에서도 백혈구 접착력 변화가 조기에 포착될 수 있음을 보여준다.
연구팀은 작동 원리를 분자 수준에서 검증하기 위해 유세포 분석(flow cytometry·형광 염색된 세포를 한 개씩 흘려보내며 레이저를 조사해, 세포 표면의 특정 단백질 발현을 빠르게 측정하는 분석 방법)도 실시했다. 분석 결과, 암이 진행된 마우스에서는 혈액 속 백혈구 가운데 PSGL-1, ESL-1, LFA-1 등 세포부착 관련 수용체가 활성화된 백혈구의 비율이 뚜렷하게 증가한 것으로 나타났다. 이 비율을 기준으로 암과 정상 상태를 구분한 ROC 분석에서는 AUC 0.982의 높은 성능을 보였다. ROC(Receiver Operating Characteristic)는 특정 지표가 양성/음성을 얼마나 잘 구분하는지를 그래프로 나타내는 방법이고, AUC(Area Under the Curve)는 ROC 아래의 면적으로, 값이 1에 가까울수록 두 집단을 이상적으로 구분할 수 있음을 뜻한다.
액체 생검을 넘어…기능적 행동을 읽는 새로운 암 모니터링 패러다임
이번 연구는 기존의 액체 생검 등을 통한 분자 농도 기반 바이오마커와 달리, 혈액에서 얻은 백혈구의 기능적 행동(롤링–부착)을 정량화해 암 상태 변화를 반영하는 지표를 제공한다는 점에서 의미가 있다. 강주헌 교수는 “영상 진단으로 발견하기 어려운 초기 전이나 재발을 환자의 백혈구 면역 반응을 통해 조기에 포착하고, 항암제 투여 이후의 치료 반응도 즉각적으로 확인할 수 있어 불필요한 치료를 줄이고 환자에게 맞는 최적의 치료제를 선별하는 데 도움을 줄 수 있다”고 설명했다.
향후 이 기술은 암의 진행 모니터링, 치료 반응 평가, 수술 후 전이·재발 감시 등 정밀 의료 기반의 환자 추적 관리에 활용될 수 있을 것으로 기대된다. 이번 연구는 UNIST 바이오메디컬공학과 브라이언 최 연구원이 제1저자로 참여했으며, UNIST, 한국연구재단 기초연구실지원사업, 과학기술정보통신부, 보건복지부, 범부처재생의료기술개발사업, 산업통상부의 지원으로 이뤄졌다.