KAIST 이노코어 연구단, 노벨화학상 수상자 데이비드 베이커와 AI 기반 단백질 설계 성공…코티솔 바이오 센서 구현
자연에 존재하지 않는 단백질을 AI로 처음부터 설계해 특정 화합물을 선택적으로 인식하고 실제 작동하는 바이오 센서로 구현하는 데 성공했다.
KAIST(총장 이광형) 생명과학과 이규리 교수는 2024년 노벨 화학상 수상자인 데이비드 베이커(David Baker) 미국 워싱턴대학교 교수와의 공동 연구를 통해 대사물질과 저분자 약물을 포함한 6종의 화합물 각각에 대해 인공 결합 단백질을 AI로 설계하고 실험적으로 검증하는 데 성공했다고 9일 밝혔다. 이번 연구 결과는 2026년 3월 28일 국제 학술지 <Nature Communications>에 게재됐다.
단백질 설계의 오랜 난제, 소분자를 알아보는 단백질을 처음부터 만든다
단백질(protein)은 아미노산이 수십~수천 개 연결된 생체 분자로, 생명 현상의 거의 모든 기능을 수행하는 핵심 부품이다. 항체가 바이러스를 인식하거나 효소가 화학 반응을 촉진하는 것 모두 단백질의 역할이다. 과학자들은 오랫동안 원하는 기능을 가진 단백질을 인공적으로 만드는 방법을 연구해 왔지만, 특히 소분자(small molecule, 아미노산·약물·호르몬처럼 분자량이 작은 화합물) 화합물을 선택적으로 인식하는 단백질을 처음부터 설계하는 것은 단백질 설계 분야에서 오랜 난제로 꼽혀 왔다.
기존 연구는 주로 자연에 이미 존재하는 단백질을 탐색하거나 그 기능 일부를 수정하는 방식에 의존했다. 이런 접근은 설계의 자유도가 제한적이어서 원하는 기능을 완전히 구현하기 어렵고, 범용적으로 적용할 수 있는 플랫폼을 만드는 데도 한계가 있었다. 이번 연구는 이러한 한계를 넘어, AI 기반 설계로 원하는 기능을 갖는 신규 단백질(de novo protein, 자연 단백질에서 출발하지 않고 처음부터 새로 설계한 단백질)을 맞춤 제작하고 실험적으로 검증까지 완료했다는 점에서 의미가 크다.
이번 연구를 이끈 이규리 교수는 2025년 2월 KAIST에 부임한 신임 교수로, 2018년부터 2024년까지 데이비드 베이커 교수 연구실(미국 워싱턴대학교, Howard Hughes Medical Institute)에서 박사후연구원 및 Staff Scientist로 연구를 수행한 바 있다. 이번 연구는 과학기술정보통신부 이노코어(InnoCORE) 사업의 AI-CRED 혁신신약 연구단의 연구 협력 기반 위에서 도출됐다.
LigandMPNN과 물리 기반 알고리즘의 융합: AI가 원자 단위로 단백질을 설계한다
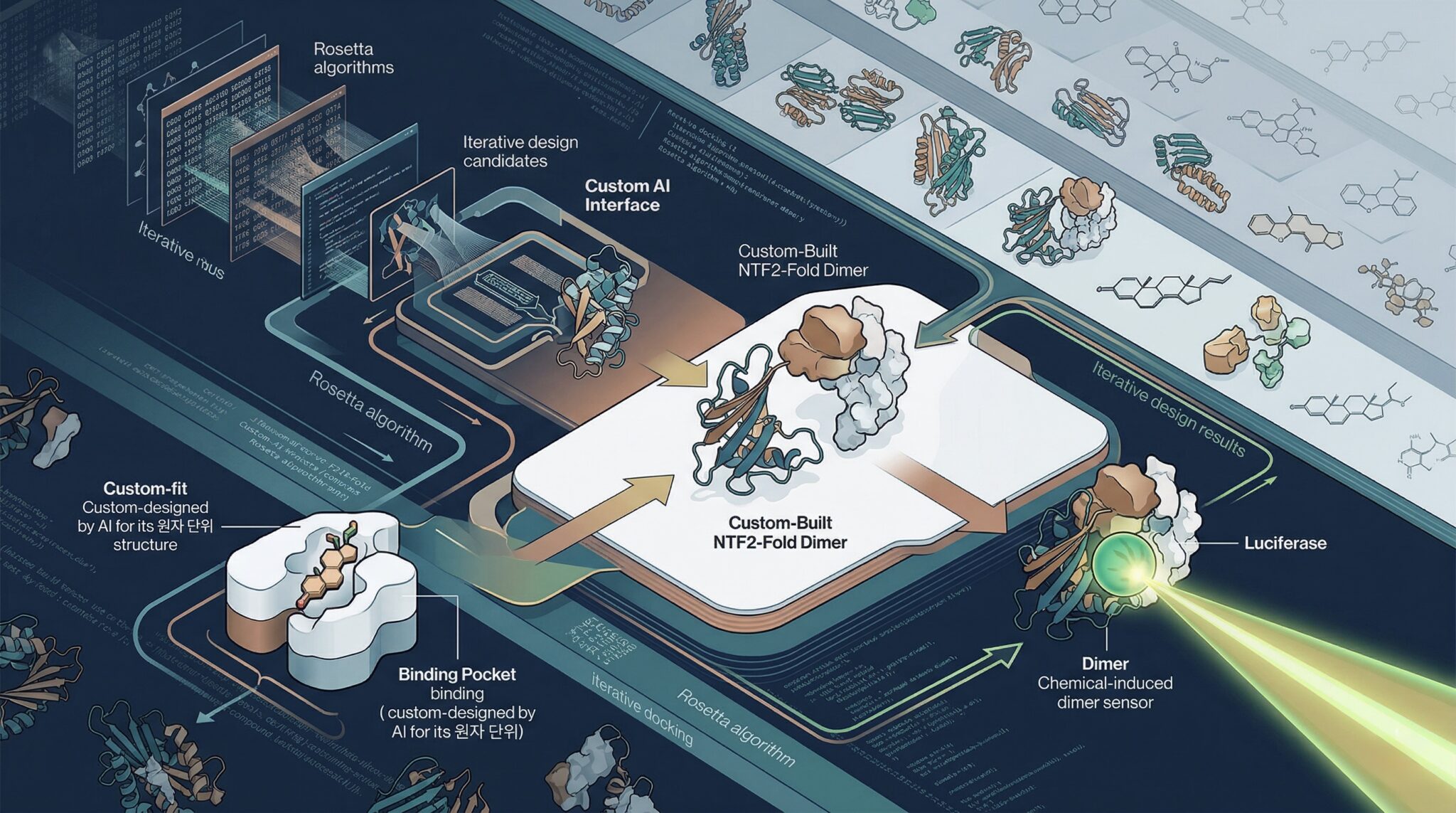
연구팀이 채택한 접근법의 핵심은 딥러닝 기반 모델과 물리화학 기반 알고리즘을 결합하는 것이다. 연구팀은 먼저 다양한 소분자 결합 설계에 범용적으로 적용할 수 있도록 결합 포켓(binding pocket, 단백질 표면에서 소분자가 끼워지는 홈 구조) 기하 구조를 다양하게 만들 수 있는 NTF2(Nuclear Transport Factor 2) 유사 단백질 폴드 뼈대 구조 라이브러리 설계 모델을 개발해 적용했다.
여기에 화합물과의 상호작용을 고려해 아미노산 서열(단백질을 구성하는 아미노산의 순서로, 단백질의 구조와 기능을 결정하는 핵심 정보)을 생성하는 딥러닝 모델 LigandMPNN을 결합했다. LigandMPNN은 같은 연구진이 개발한 모델로, 단백질이 화합물과 어떻게 상호작용할지를 고려해 최적의 아미노산 서열을 제안한다. 이 딥러닝 모델은 물리화학 기반 알고리즘인 Rosetta GALiganddock·Rosetta FastRelax와 유기적으로 결합돼 상호작용 인터페이스 설계를 더욱 정밀하게 최적화했다. 리간드 도킹(ligand docking, 저분자 화합물이 단백질의 어느 자리에 어떤 방향으로 가장 잘 결합하는지 계산으로 예측하는 방법)도 이 과정에 활용됐다.
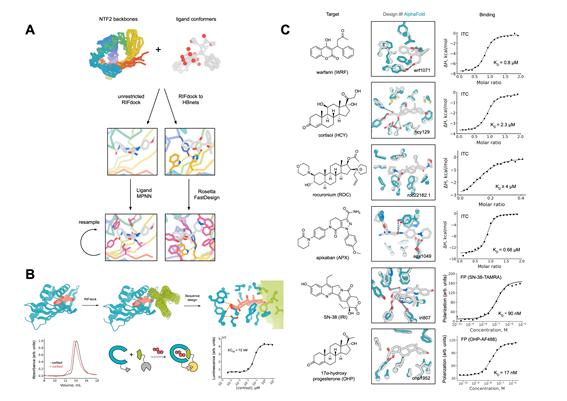
설계된 단백질 후보의 선별과 검증에는 효모 세포 표면 표현(Yeast cell surface display) 라이브러리와 형광 표지 세포 분리(FACS) 기술을 이용해 소분자 결합력을 고속으로 스크리닝했다. 설계 정확도는 소분자와 결합 단백질 복합체의 결정 구조 분석을 통해 원자 단위 해상도로 검증됐다. 그 결과 대사물질과 저분자 약물을 포함한 6종의 화합물 각각에 대해 인공 결합 단백질을 설계하고 기능을 실험적으로 확인했다.
코티솔 바이오 센서 구현과 질병 진단·신약 개발로의 확장
연구팀은 단순한 결합 단백질 설계에 그치지 않고 실제 측정 가능한 센서 기술로 확장했다. 스트레스 호르몬인 코티솔(cortisol)을 선택적으로 인식하는 신규 단백질을 설계하고, 이를 기반으로 화학 유도 이합체(chemical-induced dimer, 특정 화학물질이 결합됐을 때 두 단백질이 이합체를 형성하도록 설계된 복합체 시스템) 구조를 만들어 코티솔 바이오 센서를 개발했다. 여기에 발광 효소인 루시퍼레이즈(luciferase)를 연결해 코티솔이 결합되면 빛을 내는 방식으로 측정이 가능한 실제 센서로 구현했다. 해당 설계 기술은 미국에서 임시 특허를 출원한 상태다.
이규리 교수는 “이번 연구는 AI를 활용해 특정 화합물을 정밀하게 인식하는 단백질을 설계할 수 있음을 실험적으로 입증한 것”이라며 “앞으로 질병 진단, 신약 개발, 환경 모니터링 등 다양한 분야에서 활용될 수 있는 단백질 설계 기술로 확장해 나갈 계획”이라고 밝혔다. 혈액 속 바이오마커를 정밀하게 감지한 질병 조기 진단, 표적 치료제 개발, 환경 오염 물질을 감지하는 실시간 모니터링 센서 등으로의 응용이 기대된다.
이번 연구는 KAIST 생명과학과 이규리 교수가 제1저자로, 데이비드 베이커 교수가 교신저자로 참여했다. 논문명은 ‘Small-molecule binding and sensing with a designed protein family’이며, 이노코어 연구단과 글로벌 석학 간 협력을 통해 도출된 성과라는 점에서 의의가 있다.