UNIST·건국대병원, 노화 망막세포만 골라 제거하는 나노입자 개발…황반변성 시각 기능 회복
치료법이 제한적이었던 건성 노인성 황반변성에서 질환의 출발점인 노화 망막세포만 선택적으로 제거해 시각 기능을 회복하는 나노 약물 전달 기술이 개발됐다.
UNIST 화학과 유자형 교수와 건국대병원 안과 정혜원 교수팀은 노화된 망막색소상피세포(RPE) 표면에서만 발현이 증가하는 단백질 Bst2를 새롭게 발굴하고, 이를 표적 삼아 세포 사멸 약물을 선택적으로 전달하는 나노입자(B-Z-PON)를 개발해 실험쥐의 시각 기능을 일부 회복하는 성과를 거뒀다고 9일 밝혔다. 이번 연구 결과는 국제학술지 네이처 커뮤니케이션즈(Nature Communications)에 3월 18일자로 게재됐다.
황반변성의 근본 원인, 노화 세포가 주변까지 망가뜨린다
황반변성(Age-related Macular Degeneration, AMD)은 망막 중심부인 황반이 손상되면서 중심 시야가 흐려지거나 뒤틀려 보이는 질환으로, 백내장·녹내장과 함께 3대 실명 원인 질환으로 꼽힌다. 황반변성은 크게 건성과 습성으로 나뉘는데, 건성은 망막색소상피(Retinal Pigment Epithelium, RPE) 세포의 기능 저하와 위축이 서서히 진행되는 형태로 전체 환자의 대부분을 차지하며, 현재까지 질환 진행을 늦추는 치료에 머물러 있어 뚜렷한 표준치료법이 없다.
망막색소상피세포는 망막 가장 바깥쪽에 위치해 빛을 감지하는 시세포에 영양을 공급하고 노폐물을 처리하는 핵심 세포층이다. 이 세포는 빛에 지속적으로 노출되며 노화가 빠르게 진행되는데, 문제는 노화된 RPE가 단순히 기능을 멈추는 것이 아니라 주변에 독성 염증 물질을 뿜어내며 건강한 정상 세포까지 파괴한다는 점이다. 노화 세포가 조직 전체의 퇴행을 가속하는 이른바 ‘방관자 효과’가 황반변성의 악화 메커니즘으로 지목돼 왔다.
이런 노화 세포를 제거하는 약물군인 세놀리틱(Senolytics, 노화된 세포를 선택적으로 사멸시키는 약물의 통칭) 계열 약물이 전임상 연구에서 가능성을 보여 왔지만, 정상 세포와 노화 세포를 구분하지 못해 독성 부작용이 생기는 문제가 있었다. 특히 망막처럼 손상에 민감한 조직에서는 정상 세포를 보존하면서 노화 세포만 정밀하게 제거하는 약물 전달 기술이 절실했다.
Bst2 단백질 발굴과 이중 안전장치 나노입자 설계
연구팀은 먼저 단일세포 전사체 분석(개별 세포 하나하나의 유전자 발현 패턴을 분석하는 기술)을 통해 노화된 RPE 세포 표면에서만 발현이 증가하는 단백질 Bst2(Bone Marrow Stromal Cell Antigen 2, CD317)를 발굴했다. 자연 노화 쥐와 화학 약물로 병리적 노화를 유도한 쥐의 유전자 데이터를 교차 분석해 노화 세포 표지자로서 Bst2를 처음으로 규명한 것이다. 유자형 교수는 “노화세포 표면에만 나타나는 단백질을 새롭게 발굴해 노화세포만을 표적하는 약물 전달 나노입자를 설계할 수 있었다”고 밝혔다.
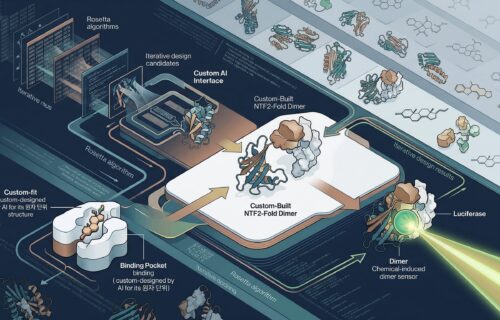
이 표지자를 기반으로 연구팀이 설계한 나노입자 B-Z-PON은 두 겹의 선택성 장치를 갖춘다. 첫 번째는 표면의 Bst2 특이 항체다. 나노입자 겉면에 Bst2 단백질에만 결합하는 항체를 장착해 노화 RPE 세포에만 선택적으로 결합한 뒤 세포 내부로 유입된다. 두 번째는 세포 내부 환경에 반응하는 약물 방출 구조다. 나노입자 내부에는 세놀리틱 약물(ABT-263)이 공유결합 형태로 연결돼 있으며, 노화 세포 특유의 고농도 글루타치온(세포 내 환원 물질) 환경에서만 이 결합이 끊어지면서 약물이 방출된다. 혹시 나노입자가 정상 세포에 잘못 전달되더라도 약물이 방출되지 않아 안전하다.
이처럼 나노입자는 표면의 항체 선택성과 세포 내 환경 감응성이라는 두 단계의 안전장치를 통해 정상 세포에는 영향을 최소화하면서 노화 세포만 선택적으로 제거하도록 설계됐다. 다공성 실리카(silica) 기반의 입자 구조는 내부에 약물을 충분히 탑재할 수 있는 공간을 제공한다.
쥐 실험에서 시각 기능 회복 확인…건성 황반변성 치료 새 방향 제시
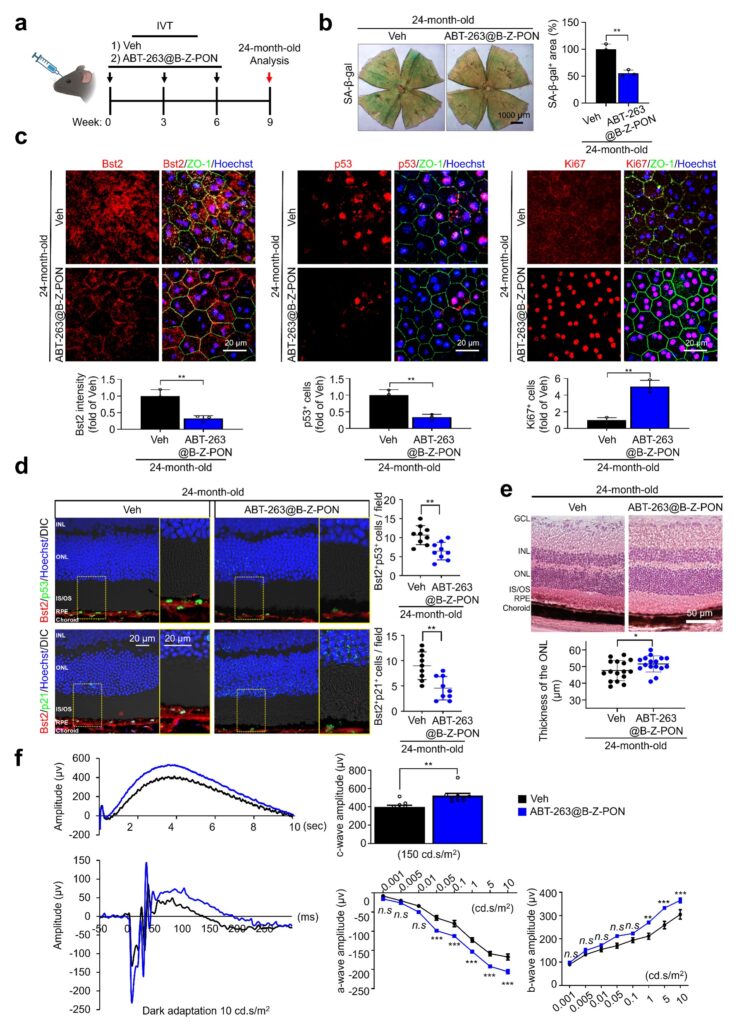
연구팀은 인위적으로 노화를 유도한 쥐 모델과 24개월령 자연 노화 쥐 모델 모두에서 약물을 탑재한 나노입자를 안구 내에 반복 주사해 효과를 검증했다. 그 결과 두 모델 모두에서 노화 세포만 선택적으로 제거되고 정상 세포는 보존되는 것이 확인됐다. 망막 조직 염색에서는 노화 세포 면적이 감소하고 세포 증식 지표(Ki67)가 증가하며 망막색소상피의 기능 회복이 나타났다.
시각 기능 회복도 측정됐다. 빛에 대한 망막의 전기적 반응을 측정하는 망막전위도(ERG, Electroretinogram) 검사에서 a-wave, b-wave, c-wave가 유의미하게 증가했으며, 망막 외핵층(시세포가 모여 있는 세포층) 두께도 유지되며 구조적 손상이 완화된 것이 확인됐다. 정혜원 교수는 “증상 완화에 머물렀던 기존 치료 방식과 달리 질환의 출발점 자체를 겨냥했다는 점에 차별점이 있다”며 “마땅한 표준치료법이 없는 건성 노인성 황반변성에서 새로운 치료 접근이 될 수 있을 것으로 기대한다”고 말했다.
연구팀은 이 기술의 확장 가능성도 강조했다. 유자형 교수는 “나노입자 표면의 특이 항체만 교체하면 다른 노인성 질환의 노화세포 표적 치료에도 활용 가능할 것”이라고 밝혔다. 논문명은 <Bst2-targeted senotherapy restores visual function by eliminating senescent retinal cells>다.